The mums2 package is designed to provide researchers with tools to analyze untargeted metabolomics data generated using tandem mass spectroscopy from microbial communities. The overall approach taken to analyze metabolomics data parallels that used to analyze microbial communities using 16S rRNA gene sequencing data. To showcase how to do this, we will demonstrate the package using a previously published database that analyzed the metabolome of Botryllus Schlosseri.
Process data
Before we begin to analyze your data, we have to process it into a
readable data.frame or object that can be viewed and
transformed. To load your data, we need to run two functions:
import_all_data(), and ms2_ms1_compare().
import_all_data() creates an object reflecting MS1 data,
and ms2_ms1_compare()assigns MS2 spectra to your MS1 data.
At this point, you may need to filter out noise or transform certain
parameters before you can properly analyze your data. To accommodate for
those issues, we have two other functions:
filter_peak_table(), and
change_rt_to_seconds_or_minute().
filter_peak_table() allows your to remove low-quality
features and change_rt_to_seconds_or_minute() allows you to
transform your retention time to minutes or seconds. This allows you to
ensure that the retention time in your MS1 data matches your MS2 data.
Below will explain what each function does in more detail and illustrate
how to go through the pipeline.
Import
The import_all_data() function takes in a peak_table and
meta_data tables as input and converts them into an mpactr
object (this is a wrapper for mpactr::import_data()). The
format parameter accepts three different formats: Metaboscape,
Progenesis, and None. You can read up more about each of the formats
here(mpactr::import_data()). If you need a deeper
understanding of what format the peak_table and meta_data files should
be in, take a look at mpactr’s getting started
page.
meta_data is a csv that provides information about the samples. In
order for your meta_data to be valid, it needs the following columns:
“Injection”, “Sample_Code”, ”Biological_Group”. The values in the
“Injection” column should match the sample injection columns inside of
the peak_table. “Sample_Code” is the ID of your technical replicates.
Finally, “Biological_Group” is the ID of your biological replicate
groups (you can learn more about the meta_data file format here
mpactr::import_data()).
data <- import_all_data(
peak_table = mums2::mums2_example("230112_botryllus_peaktable.csv"),
meta_data = mums2::mums2_example("meta_data_boryillus.csv"),
format = "Progenesis")Peak Table
Below is the expected format for a progenesis peak table. It contains samples as columns and features as rows. The feature intensities are expected to be un-normalized.
read.csv(mums2::mums2_example("230112_botryllus_peaktable.csv"), check.names = FALSE)
#> Raw abundance
#>
#> [ reached 'max' / getOption("max.print") -- omitted 8 columns ]
#> [ reached 'max' / getOption("max.print") -- omitted 12824 rows ]Metadata
The expected format for metadata is below. The metadata file needs to contain at minimum columns for “Injection”, “Sample_Code”, and ”Biological_Group”.
read.csv(mums2::mums2_example("meta_data_boryillus.csv"), check.names = FALSE)
#> Injection File Text Sample_Notes MS method LC method
#> 1 221012_DGM_Blank1_1_1_390 NA NA NA NA
#> 2 221012_DGM_Blank1_1_2_391 NA NA NA NA
#> 3 221012_DGM_Blank1_1_3_392 NA NA NA NA
#> 4 221012_DGM_MB1588_3_1_395 NA NA NA NA
#> Vial_Position Injection volume Sample_Code Biological_Group
#> 1 NA 2 blank Blanks
#> 2 NA 2 blank Blanks
#> 3 NA 2 blank Blanks
#> 4 NA 2 MB1588 botryllus
#> [ reached 'max' / getOption("max.print") -- omitted 41 rows ]Filter
After importing the data, you can use functions from mpactR to filter
the data. There are four different filters in the mpactR package:
mpactr::filter_mispicked_ions(),
mpactr::filter_group(), mpactr::filter_cv(),
and mpactr::filter_insource_ions() (You can find more
information on mpactR’s
website). Although data filtering is not required, it will help reduce
noise and correct peak selection errors, which will also speed up the
analysis.
filtered_data <- data |>
filter_peak_table(filter_mispicked_ions_params()) |>
filter_peak_table(filter_cv_params(cv_threshold = 0.2)) |>
filter_peak_table(filter_group_params(group_threshold = 0.1,
"Blanks")) |>
filter_peak_table(filter_insource_ions_params())
#> ℹ Checking 12822 peaks for mispicked peaks.
#> ℹ Argument merge_peaks is: TRUE. Merging mispicked peaks with method sum.
#> ✔ 2429 ions failed the mispicked filter, 10393 ions remain.
#> ℹ Parsing 10393 peaks for replicability across technical replicates.
#> ✔ 2229 ions failed the cv_filter filter, 8164 ions remain.
#> ℹ Parsing 8164 peaks based on the sample group: Blanks.
#> ℹ Argument remove_ions is: TRUE.Removing peaks from Blanks.
#> ✔ 2538 ions failed the Blanks filter, 5626 ions remain.
#> ℹ Parsing 5626 peaks for insource ions.
#> ✔ 1082 ions failed the insource filter, 4544 ions remain.
head(get_peak_table(filtered_data), 3)
#> Key: <Compound, mz, kmd, rt>
#> Compound mz kmd rt 221012_DGM_Blank1_1_1_390
#> <char> <num> <num> <num> <num>
#> 1: 1000.05311 Da 399.15 s 1001.060 0.06039 6.65 0
#> 2: 1000.20067 Da 536.14 s 1001.208 0.20795 8.94 0
#> 3: 1000.54504 Da 353.23 s 1023.534 0.53397 5.89 0
#> 221012_DGM_Blank1_1_2_391 221012_DGM_Blank1_1_3_392
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_Blank2_1_1_404 221012_DGM_Blank2_1_2_405
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_Blank2_1_3_406 221012_DGM_Blank3_1_1_419
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_Blank3_1_2_420 221012_DGM_Blank3_1_3_421
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_Blank4_1_1_434 221012_DGM_Blank4_1_2_435
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_Blank4_1_3_436 221012_DGM_MB1588_3_1_395
#> <num> <num>
#> 1: 0 0.00
#> 2: 0 13693.07
#> 3: 0 0.00
#> 221012_DGM_MB1588_3_2_396 221012_DGM_MB1588_3_3_397
#> <num> <num>
#> 1: 0.00 0.00
#> 2: 16856.57 16332.37
#> 3: 0.00 0.00
#> 221012_DGM_MB1589_4_1_398 221012_DGM_MB1589_4_2_399
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1589_4_3_400 221012_DGM_MB1590_5_1_401
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1590_5_2_402 221012_DGM_MB1590_5_3_403
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1591_6_1_407 221012_DGM_MB1591_6_2_408
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1591_6_3_409 221012_DGM_MB1592_7_1_410
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1592_7_2_411 221012_DGM_MB1592_7_3_412
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1593_8_1_413 221012_DGM_MB1593_8_2_414
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1593_8_3_415 221012_DGM_MB1594_9_1_416
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1594_9_2_417 221012_DGM_MB1594_9_3_418
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1595_10_1_422 221012_DGM_MB1595_10_2_423
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1595_10_3_424 221012_DGM_MB1597_11_1_425
#> <num> <num>
#> 1: 0 15105.36
#> 2: 0 0.00
#> 3: 0 168557.48
#> 221012_DGM_MB1597_11_2_426 221012_DGM_MB1597_11_3_427
#> <num> <num>
#> 1: 13140.04 17551.49
#> 2: 0.00 0.00
#> 3: 176505.77 160923.45
#> 221012_DGM_MB1598_12_1_428 221012_DGM_MB1598_12_2_429
#> <num> <num>
#> 1: 0 0
#> 2: 0 0
#> 3: 0 0
#> 221012_DGM_MB1598_12_3_430 221012_DGM_MB1599_13_1_431
#> <num> <num>
#> 1: 0 13573.71
#> 2: 0 0.00
#> 3: 0 153978.06
#> 221012_DGM_MB1599_13_2_432 221012_DGM_MB1599_13_3_433 cor
#> <num> <num> <lgcl>
#> 1: 13245.09 13221.95 TRUE
#> 2: 0.00 0.00 TRUE
#> 3: 158672.23 165991.44 TRUEConvert retention time to “rt in minutes” or “rt in seconds”
Sometimes an MS2 file will report the retention time in minutes but
the MS1 file will report in seconds. This mismatch will cause incorrect
peak matching between MS1 and MS2 data. The
change_rt_to_seconds_or_minute() function allows users to
synthesize data with different units. Be aware that this function
modifies the mpactr object in place. Therefore, you will need to call
the function again to revert the units. Below will display a vector of
retention time.
get_peak_table(filtered_data)$rt
#> [1] 6.65 8.94 5.89 6.86 6.98 5.91 10.07 7.35 6.91 6.67 6.68 7.38
#> [13] 5.81 4.79 7.48
#> [ reached 'max' / getOption("max.print") -- omitted 4529 entries ]
filtered_data <- change_rt_to_seconds_or_minute(mpactr_object = filtered_data, rt_type = "seconds")
#> [1] "Changing rt values to seconds"
head(get_peak_table(filtered_data), 1)
#> Key: <Compound, mz, kmd, RTINSECONDS>
#> Compound mz kmd RTINSECONDS 221012_DGM_Blank1_1_1_390
#> <char> <num> <num> <num> <num>
#> 1: 1000.05311 Da 399.15 s 1001.06 0.06039 399 0
#> 221012_DGM_Blank1_1_2_391 221012_DGM_Blank1_1_3_392
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank2_1_1_404 221012_DGM_Blank2_1_2_405
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank2_1_3_406 221012_DGM_Blank3_1_1_419
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank3_1_2_420 221012_DGM_Blank3_1_3_421
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank4_1_1_434 221012_DGM_Blank4_1_2_435
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank4_1_3_436 221012_DGM_MB1588_3_1_395
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1588_3_2_396 221012_DGM_MB1588_3_3_397
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1589_4_1_398 221012_DGM_MB1589_4_2_399
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1589_4_3_400 221012_DGM_MB1590_5_1_401
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1590_5_2_402 221012_DGM_MB1590_5_3_403
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1591_6_1_407 221012_DGM_MB1591_6_2_408
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1591_6_3_409 221012_DGM_MB1592_7_1_410
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1592_7_2_411 221012_DGM_MB1592_7_3_412
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1593_8_1_413 221012_DGM_MB1593_8_2_414
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1593_8_3_415 221012_DGM_MB1594_9_1_416
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1594_9_2_417 221012_DGM_MB1594_9_3_418
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1595_10_1_422 221012_DGM_MB1595_10_2_423
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1595_10_3_424 221012_DGM_MB1597_11_1_425
#> <num> <num>
#> 1: 0 15105.36
#> 221012_DGM_MB1597_11_2_426 221012_DGM_MB1597_11_3_427
#> <num> <num>
#> 1: 13140.04 17551.49
#> 221012_DGM_MB1598_12_1_428 221012_DGM_MB1598_12_2_429
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1598_12_3_430 221012_DGM_MB1599_13_1_431
#> <num> <num>
#> 1: 0 13573.71
#> 221012_DGM_MB1599_13_2_432 221012_DGM_MB1599_13_3_433 cor
#> <num> <num> <lgcl>
#> 1: 13245.09 13221.95 TRUE
filtered_data <- change_rt_to_seconds_or_minute(mpactr_object = filtered_data, rt_type = "minutes")
#> [1] "Changing rt values to minutes"
head(get_peak_table(filtered_data), 1)
#> Key: <Compound, mz, kmd, RTINMINUTES>
#> Compound mz kmd RTINMINUTES 221012_DGM_Blank1_1_1_390
#> <char> <num> <num> <num> <num>
#> 1: 1000.05311 Da 399.15 s 1001.06 0.06039 6.65 0
#> 221012_DGM_Blank1_1_2_391 221012_DGM_Blank1_1_3_392
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank2_1_1_404 221012_DGM_Blank2_1_2_405
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank2_1_3_406 221012_DGM_Blank3_1_1_419
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank3_1_2_420 221012_DGM_Blank3_1_3_421
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank4_1_1_434 221012_DGM_Blank4_1_2_435
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank4_1_3_436 221012_DGM_MB1588_3_1_395
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1588_3_2_396 221012_DGM_MB1588_3_3_397
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1589_4_1_398 221012_DGM_MB1589_4_2_399
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1589_4_3_400 221012_DGM_MB1590_5_1_401
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1590_5_2_402 221012_DGM_MB1590_5_3_403
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1591_6_1_407 221012_DGM_MB1591_6_2_408
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1591_6_3_409 221012_DGM_MB1592_7_1_410
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1592_7_2_411 221012_DGM_MB1592_7_3_412
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1593_8_1_413 221012_DGM_MB1593_8_2_414
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1593_8_3_415 221012_DGM_MB1594_9_1_416
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1594_9_2_417 221012_DGM_MB1594_9_3_418
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1595_10_1_422 221012_DGM_MB1595_10_2_423
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1595_10_3_424 221012_DGM_MB1597_11_1_425
#> <num> <num>
#> 1: 0 15105.36
#> 221012_DGM_MB1597_11_2_426 221012_DGM_MB1597_11_3_427
#> <num> <num>
#> 1: 13140.04 17551.49
#> 221012_DGM_MB1598_12_1_428 221012_DGM_MB1598_12_2_429
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1598_12_3_430 221012_DGM_MB1599_13_1_431
#> <num> <num>
#> 1: 0 13573.71
#> 221012_DGM_MB1599_13_2_432 221012_DGM_MB1599_13_3_433 cor
#> <num> <num> <lgcl>
#> 1: 13245.09 13221.95 TRUEPreprocess MS2 data
We can use a .mgf/.mzxml/.mzml file to match MS2 spectra to MS1
peaks. The ms2_ms1_compare() function reads a list of mgf
files and matches them to a MS1 feature based on the mass-to-charge
ratio and retention time tolerance. If there are multiple matches, this
function will select the MS2 spectra with the highest intensity. Keep in
mind that MS2 spectra files are very memory intensive, they can be
anywhere from 1 MB to 100 GB. Therefore, depending on how big the file
is, it might take a few moments for the function to complete.
ms2_ms1_compare() generates a list of data with two
data.frames (“ms1_data”, “peak_data”), a list (“peak_data”), and a
character vector (“samples”).
ms2_matches - One of the two data.frames, “ms2_matches”, is a data.frame that contains five columns: “mz”, “rt”, “ms1_compound_id”, “spectra_index”, and “ms2_spectrum_id.” “mz” and “rt” are reported from the MS2 file as mass-to-charge ratio and retention time, respectively. “ms1_compound_id” is the compound id that was imported from the MS1 peak_table. “spectra_index” matches the MS2 data with its MS2 spectrum. Finally, “ms2_spectrum_id” is the generated name to represent your MS2 spectra (combination of your mz and rt). This is necessary to properly compare compounds. Since compounds with similar structures are expected to have similar MS2 patterns, we can use algorithmic techniques to compute the similarity between two spectra. This allows us to generate annotations and cluster similar spectra together.
ms1_data - The other “data.frame”, “ms1_data”, is a data.frame of the created mpactr object.
peak_data - The list that is generate from
ms2_ms1_compare() is named “peak_data.” “peak_data” is a
collection of MS2 peak list. A peak list a collection of fragment ions,
they all have a value to represent their intensity and mass-charge
ratio.
samples - The last slot inside of the list is a character vector named “samples.” This is a list of the groups/samples contained inside of your peak_table file.
matched_data <- ms2_ms1_compare(
ms2_files = mums2_example("botryllus_v2.gnps.mgf"),mpactr_object = filtered_data, mz_tolerance = 5, rt_tolerance = 6)
#> [1] "Reading: /home/runner/work/_temp/Library/mums2/extdata/botryllus_v2.gnps.mgf ..."
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
#> [1] "674/4544 peaks have an MS2 spectra."
head(matched_data$ms2_matches)
#> mz rt ms1_compound_id spectra_index ms2_spectrum_id
#> 1 1023.533 5.89 1000.54504 Da 353.23 s 1 mz1023.53293rt5.89
#> 2 1002.552 5.89 1001.54432 Da 354.35 s 2 mz1002.55208rt5.89
#> 3 1008.593 5.54 1007.58494 Da 332.99 s 3 mz1008.59344rt5.54
#> 4 515.367 6.40 1028.72044 Da 383.88 s 4 mz515.36698rt6.4
#> 5 1046.580 5.91 1045.57237 Da 354.13 s 5 mz1046.57957rt5.91
#> 6 524.361 6.67 1046.70233 Da 400.23 s 6 mz524.36102rt6.67
head(matched_data$ms1_data, 1)
#> Key: <Compound, mz, kmd, RTINMINUTES>
#> Compound mz kmd RTINMINUTES 221012_DGM_Blank1_1_1_390
#> <char> <num> <num> <num> <num>
#> 1: 1000.05311 Da 399.15 s 1001.06 0.06039 6.65 0
#> 221012_DGM_Blank1_1_2_391 221012_DGM_Blank1_1_3_392
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank2_1_1_404 221012_DGM_Blank2_1_2_405
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank2_1_3_406 221012_DGM_Blank3_1_1_419
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank3_1_2_420 221012_DGM_Blank3_1_3_421
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank4_1_1_434 221012_DGM_Blank4_1_2_435
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_Blank4_1_3_436 221012_DGM_MB1588_3_1_395
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1588_3_2_396 221012_DGM_MB1588_3_3_397
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1589_4_1_398 221012_DGM_MB1589_4_2_399
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1589_4_3_400 221012_DGM_MB1590_5_1_401
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1590_5_2_402 221012_DGM_MB1590_5_3_403
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1591_6_1_407 221012_DGM_MB1591_6_2_408
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1591_6_3_409 221012_DGM_MB1592_7_1_410
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1592_7_2_411 221012_DGM_MB1592_7_3_412
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1593_8_1_413 221012_DGM_MB1593_8_2_414
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1593_8_3_415 221012_DGM_MB1594_9_1_416
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1594_9_2_417 221012_DGM_MB1594_9_3_418
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1595_10_1_422 221012_DGM_MB1595_10_2_423
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1595_10_3_424 221012_DGM_MB1597_11_1_425
#> <num> <num>
#> 1: 0 15105.36
#> 221012_DGM_MB1597_11_2_426 221012_DGM_MB1597_11_3_427
#> <num> <num>
#> 1: 13140.04 17551.49
#> 221012_DGM_MB1598_12_1_428 221012_DGM_MB1598_12_2_429
#> <num> <num>
#> 1: 0 0
#> 221012_DGM_MB1598_12_3_430 221012_DGM_MB1599_13_1_431
#> <num> <num>
#> 1: 0 13573.71
#> 221012_DGM_MB1599_13_2_432 221012_DGM_MB1599_13_3_433 cor
#> <num> <num> <lgcl>
#> 1: 13245.09 13221.95 TRUE
matched_data$peak_data[[1]]
#> $mz
#> [1] 1022.596 1023.534 1024.468 1024.540 1024.590 1025.538 1025.577 1025.880
#> [9] 1026.543
#>
#> $intensity
#> [1] 88.035540 3698.286100 37.559235 1735.583300 43.992560 803.445070
#> [7] 159.595730 8.381788 224.810270
matched_data$samples
#> [1] "221012_DGM_Blank1_1_1_390" "221012_DGM_Blank1_1_2_391"
#> [3] "221012_DGM_Blank1_1_3_392" "221012_DGM_MB1588_3_1_395"
#> [5] "221012_DGM_MB1588_3_2_396" "221012_DGM_MB1588_3_3_397"
#> [7] "221012_DGM_MB1589_4_1_398" "221012_DGM_MB1589_4_2_399"
#> [9] "221012_DGM_MB1589_4_3_400" "221012_DGM_MB1590_5_1_401"
#> [11] "221012_DGM_MB1590_5_2_402" "221012_DGM_MB1590_5_3_403"
#> [13] "221012_DGM_Blank2_1_1_404" "221012_DGM_Blank2_1_2_405"
#> [15] "221012_DGM_Blank2_1_3_406" "221012_DGM_MB1591_6_1_407"
#> [17] "221012_DGM_MB1591_6_2_408" "221012_DGM_MB1591_6_3_409"
#> [19] "221012_DGM_MB1592_7_1_410" "221012_DGM_MB1592_7_2_411"
#> [21] "221012_DGM_MB1592_7_3_412" "221012_DGM_MB1593_8_1_413"
#> [23] "221012_DGM_MB1593_8_2_414" "221012_DGM_MB1593_8_3_415"
#> [25] "221012_DGM_MB1594_9_1_416" "221012_DGM_MB1594_9_2_417"
#> [27] "221012_DGM_MB1594_9_3_418" "221012_DGM_Blank3_1_1_419"
#> [29] "221012_DGM_Blank3_1_2_420" "221012_DGM_Blank3_1_3_421"
#> [31] "221012_DGM_MB1595_10_1_422" "221012_DGM_MB1595_10_2_423"
#> [33] "221012_DGM_MB1595_10_3_424" "221012_DGM_MB1597_11_1_425"
#> [35] "221012_DGM_MB1597_11_2_426" "221012_DGM_MB1597_11_3_427"
#> [37] "221012_DGM_MB1598_12_1_428" "221012_DGM_MB1598_12_2_429"
#> [39] "221012_DGM_MB1598_12_3_430" "221012_DGM_MB1599_13_1_431"
#> [41] "221012_DGM_MB1599_13_2_432" "221012_DGM_MB1599_13_3_433"
#> [43] "221012_DGM_Blank4_1_1_434" "221012_DGM_Blank4_1_2_435"
#> [45] "221012_DGM_Blank4_1_3_436"Generate Metadata
Once you have preprocessed your data, we can start to generate
additional metadata like molecular formulas and annotations.
compute_molecular_formulas() allows us to generate
molecular formulas and annotate_ms2() allows us to annotate
our data based on reference databases. This allows us to confirm known
features and annotate additional metadata to unknown features. Below
will explain in further detail how these functions can be used.
Molecular formula prediction
mums2 can generate de novo molecular formula predictions using
fragmentation trees. The compute_molecular_formulas()
function uses MS2 data to generate the most explained molecular formula
and return it as a result (for more information: Fragmentation
Trees). The most explained molecular formula simply means the
molecular formula that is explained by the most peaks in the spectra. In
order to create a fragmentation tree, we generate candidate formulas
that comprise of every possible molecular formula the parent mass can
create (using only CHNOPS). We then look at every mass and intensity
pair inside of the spectra and compute every molecular formula. We then
create a one directional graph based on all the molecular formulas
using. A molecular formula will point to another if it is a subformula
of another formula (meaning it contains at most as many atoms as the
parent formula). Finally, we can compute a score for each one of the
nodes using methods like Ring Double Bond equivalents, compute molecular
formula score, etc. You can learn how other open-sourced software such
as MZMine and Sirius generate molecular
formula. Due to the time this function will take to run, we are going to
use a small testset.
It is possible for a formula to be unable to be generated. In this case, we return an NA to represent an unknown molecular formula.
Warning messages will be printed if no molecular formula is generated or there is only one possible molecular formula.
data_small <- import_all_data(
peak_table = mums2::mums2_example("botryllus_pt_small.csv"),
meta_data = mums2::mums2_example("meta_data_boryillus.csv"),
format = "None") |>
filter_peak_table(filter_mispicked_ions_params()) |>
filter_peak_table(filter_cv_params(cv_threshold = 0.05)) |>
filter_peak_table(filter_group_params(group_threshold = 0.1,
"Blanks")) |>
filter_peak_table(filter_insource_ions_params())
#> ℹ Checking 1500 peaks for mispicked peaks.
#> ℹ Argument merge_peaks is: TRUE. Merging mispicked peaks with method sum.
#> ✔ 50 ions failed the mispicked filter, 1450 ions remain.
#> ℹ Parsing 1450 peaks for replicability across technical replicates.
#> ✔ 1112 ions failed the cv_filter filter, 338 ions remain.
#> ℹ Parsing 338 peaks based on the sample group: Blanks.
#> ℹ Argument remove_ions is: TRUE.Removing peaks from Blanks.
#> ✔ 67 ions failed the Blanks filter, 271 ions remain.
#> ℹ Parsing 271 peaks for insource ions.
#> ✔ 10 ions failed the insource filter, 261 ions remain.
matched_data_small <- ms2_ms1_compare(
ms2_files = mums2_example("botryllus_v2.gnps.mgf"), mpactr_object = data_small, mz_tolerance = .5, rt_tolerance = 6)
#> [1] "Reading: /home/runner/work/_temp/Library/mums2/extdata/botryllus_v2.gnps.mgf ..."
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
#> [1] "9/261 peaks have an MS2 spectra."
matched_data_small <- compute_molecular_formulas(mass_data = matched_data_small, parent_ppm = 3)
#> Calculating decomposition masses...
#> Computing | 11% ETA: -...Computing ■■■■■ | 11% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 33% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 55% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
#> Calculating fragmentation trees...
#> Computing | 11% ETA: -...Computing ■■■■■ | 11% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 33% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 55% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
#> 9/9 chemical formulas were predicted
matched_data_small$predicted_molecular_formulas
#> [1] "C40H192N7O5P3S4" "C9H185N6O6PS" "C10H187N5O5P2S2" "C6H183N2O5PS2"
#> [5] "C10H61N7O9P2S" "C11H58N6O4P4S2" "C6H99N5O6P6S2" "C17H68N5O6P3S2"
#> [9] "C17H57N13O17P2S3"Annotations
Beyond predicting the molecular formula, we can also use the
annotate_ms2() function to annotate the data in the
matched_ms2_ms1 object using reference databases. A reference database
can be input as msp files using the read_msp() function. It
returns a reference database that can be used as an input for the
annotate_ms2() function. In the mums2 package, MS2 spectral
similarity can be determined using either spectral entropy (for more
information: Spectral Entropy)
or gnps algorithm (for more information: GNPS). While gnps uses a
modified cosine score to compute similarity between spectra, spectral
entropy takes advantage of the total intensities of the spectra. The
chosen method can be used by supplying either, gnps_param()
or spec_entropy_params(). Using these two methods, we can
effectively generate a collection of annotations based on the reference
databases. We have a small massbank database provided from MSDial
on 05/12/2026 that is preloaded in the package and can be used to
annotate data.
reference_db <- read_msp(msp_file = mums2_example("massbank_example_data.msp"))
#> [1] "Reading: /home/runner/work/_temp/Library/mums2/extdata/massbank_example_data.msp ..."
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
annotations <- annotate_ms2(
mass_data = matched_data, reference = reference_db,
scoring_params = modified_cosine_params(0.5), ppm = 1000,
min_score = 0.1, chemical_min_score = 0)
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
annotations[1:5,]
#> query_ms1_id query_ms2_id query_mz query_rt ref_idx
#> 1 1028.72044 Da 383.88 s mz515.36698rt6.4 515.366980 6.400000 3283
#> 2 1028.72044 Da 383.88 s mz515.36698rt6.4 515.366980 6.400000 3284
#> 3 1028.72044 Da 383.88 s mz515.36698rt6.4 515.366980 6.400000 3289
#> 4 1028.72044 Da 383.88 s mz515.36698rt6.4 515.366980 6.400000 3290
#> 5 1050.56754 Da 368.94 s mz1051.57522rt6.15 1051.575220 6.150000 5777
#> query_formula chemical_similarity score collisionenergy instrument
#> 1 0.000000 0.166047 15
#> 2 0.000000 0.164341 30
#> 3 0.000000 0.167768 15
#> 4 0.000000 0.159757 30
#> 5 0.000000 0.476564 0.0
#> instrumenttype comment ionmode ccs
#> 1 LC-ESI-ITFT registered in MassBank Positive 229.5588665
#> 2 LC-ESI-ITFT registered in MassBank Positive 229.5588665
#> 3 LC-ESI-ITFT registered in MassBank Positive 229.5588665
#> 4 LC-ESI-ITFT registered in MassBank Positive 229.5588665
#> 5 LC-ESI-ITFT registered in MassBank Positive -1
#> smiles
#> 1 CCCC1=NC2=C(C=C(C=C2C)C2=NC3=CC=CC=C3N2C)N1CC1=CC=C(C=C1)C1=CC=CC=C1C(O)=O
#> 2 CCCC1=NC2=C(C=C(C=C2C)C2=NC3=CC=CC=C3N2C)N1CC1=CC=C(C=C1)C1=CC=CC=C1C(O)=O
#> 3 CCCC1=NC2=C(C=C(C=C2C)C2=NC3=CC=CC=C3N2C)N1CC1=CC=C(C=C1)C1=CC=CC=C1C(O)=O
#> 4 CCCC1=NC2=C(C=C(C=C2C)C2=NC3=CC=CC=C3N2C)N1CC1=CC=C(C=C1)C1=CC=CC=C1C(O)=O
#> 5 OCC1O[C@@H](OC2=CC=C(\\C=C\\C(=O)OCC3O[C@@H](OC4=C([O+]=C5C=C(O)C=C(O[C@@H]6OC(CO)[C@@H](O)C(O)[C@@H]6O)C5=C4)C4=CC(O)=C(O)C=C4)[C@@H](O[C@@H]4OC[C@@H](O)[C@@H](O)C4O)C(O)[C@@H]3O)C=C2)[C@@H](O)C(O)[C@@H]1O
#> inchikey retentiontime precursortype num.peaks
#> 1 RMMXLENWKUUMAY-UHFFFAOYSA-N [M+H]+ 2
#> 2 RMMXLENWKUUMAY-UHFFFAOYSA-N [M+H]+ 4
#> 3 RMMXLENWKUUMAY-UHFFFAOYSA-N [M+H]+ 2
#> 4 RMMXLENWKUUMAY-UHFFFAOYSA-N [M+H]+ 5
#> 5 OPWPCWHMCUWCGG-XKYKWVHPSA-O [M]+ 4
#> name
#> 1 Telmisartan; LC-ESI-ITFT; MS2; CE
#> 2 Telmisartan; LC-ESI-ITFT; MS2; CE
#> 3 Telmisartan; LC-ESI-ITFT; MS2; CE
#> 4 Telmisartan; LC-ESI-ITFT; MS2; CE
#> 5 Cyanidin 3-O-[2''-O-(xylosyl)-6''-O-(p-O-(glucosyl)-p-coumaroyl) glucoside] 5-O-glucoside; LC-ESI-ITFT; MS2; CE 0.0 eV; [M]+
#> ontology precursormz formula
#> 1 Biphenyls and derivatives 515.244153 C33H30N4O2
#> 2 Biphenyls and derivatives 515.244153 C33H30N4O2
#> 3 Biphenyls and derivatives 515.244153 C33H30N4O2
#> 4 Biphenyls and derivatives 515.244153 C33H30N4O2
#> 5 Anthocyanidin 3-O-6-p-coumaroyl glycosides 1051.291974 C47H55O27Create OMUs
Let’s look into generating OMUs. OMUs are cluster of metabolites with
similar MS2 spectral patterns and can be used for numerous analyses. To
properly cluster your data together, you need to generate some
similarity or distance between the features of your data. This is where
our dist_ms2() function comes in. After you generate a
distance data.frame we can use the
cluster_data() function to create your OMUs. Below will
show you the process how this works.
Scoring/Distance
We have implemented two different distance calculations to generate
distances between compounds. To generate the distances you can use the
gnps algorithm (modified_cosine_params()) or spectral
entropy algorithm (spec_entropy_params()). Just like above,
being able to compute the similarity between MS2 spectra is what allows
us to cluster data. We can also use the similarity distances to generate
a simple distance data.frame for later use.
dist <- dist_ms2(
data = matched_data, cutoff = 0.3, precursor_threshold = -1,
score_params = modified_cosine_params(0.5), min_peaks = 0)
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
dist
#> i j dist
#> 1 1 2 0.05989299
#> 2 1 3 0.06767390
#> 3 1 5 0.06993205
#> 4 1 506 0.24147716
#> 5 1 341 0.19118126
#> [ reached 'max' / getOption("max.print") -- omitted 59729 rows ]Operational Metabolomic Units (OMUs)
OMUs, or Operational Metabolomic Units, are clusters of metabolomic
features. We cluster these features based on how similar their MS2
spectra are to each other. The dist_ms2() function
generates a distance data.frame, or a
data.frame of closeness between metabolomic features. Using
the generated object along with the matched_ms2_ms1 object, we are able
to cluster the features to generate OMUs using the
cluster_data() function. This function returns a list with
five slots: label, abundance, cluster, cluster_metrics, and
iteration_metrics.
label - Represents the cutoff distance used for the
cluster. abundance - A data.frame() that
shows the absolute abundance of the clusters by sample.
cluster - A data.frame() that shows which
features clustered together by cluster ID.
cluster_metrics - A data.frame()
representing metrics for how the clusters were formed.
iteration_metrics - A data.frame() that
shows how the features was clustered at each iteration.
cluster_results <- cluster_data(
distance_df = dist, ms2_match_data = matched_data, cutoff = 0.3,
cluster_method = "opticlust")
cluster_results
#> $label
#> [1] 0.3
#>
#> $abundance
#> samples omu abundance
#> 1 221012_DGM_Blank4_1_2_435 omu1 0.00
#> 2 221012_DGM_Blank4_1_1_434 omu1 0.00
#> 3 221012_DGM_MB1599_13_3_433 omu1 48932.22
#> 4 221012_DGM_MB1599_13_1_431 omu1 48982.59
#> 5 221012_DGM_MB1598_12_3_430 omu1 0.00
#> [ reached 'max' / getOption("max.print") -- omitted 5440 rows ]
#>
#> $cluster
#> feature omu
#> 1 1028.72044 Da 383.88 s omu1
#> 2 1046.70233 Da 400.23 s omu2
#> 3 1067.55304 Da 352.68 s omu3
#> 4 1072.74610 Da 382.97 s omu4
#> 5 1076.25679 Da 479.00 s omu5
#> 6 1083.57570 Da 350.99 s omu6
#> 7 1127.60610 Da 352.16 s omu7
#> [ reached 'max' / getOption("max.print") -- omitted 114 rows ]
#>
#> $cluster_metrics
#> label cutoff specificity ppv ttp f1score tn
#> 1 0.300000 0.300000 0.963847 0.889087 48417.000000 0.848000 161027.000000
#> mcc fn fp sensitivity npv fdr accuracy
#> 1 0.798530 11317.000000 6040.000000 0.810543 0.934335 0.889087 0.923470
#>
#> $iteration_metrics
#> iter time label num_otus cutoff tp tn fp fn sensitivity specificity ppv
#> npv fdr accuracy
#> [ reached 'max' / getOption("max.print") -- omitted 2 columns ]
#> [ reached 'max' / getOption("max.print") -- omitted 5 rows ]
#>
#> attr(,"class")
#> [1] "mothur_cluster"Display OMUs when you annotate
After your data has been clustered, if you wish to see which OMUs the
annotated features are in, you can supply that to the annotation
function using the “cluster_data” parameter. Doing so will add a column
named OMU to the annotations result data.frame. This column
will display the OMU the feature is represented in.
annotations <- annotate_ms2(mass_data = matched_data, reference = reference_db, scoring_params = modified_cosine_params(0.5),
ppm = 1000, min_score = 0.7, chemical_min_score = 0, cluster_data = cluster_results)
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
annotations[1:5,]
#> query_ms1_id query_ms2_id query_mz query_rt ref_idx
#> 1 1088.53252 Da 351.76 s mz545.27303rt7.97 545.273030 7.970000 3762
#> 2 1088.53252 Da 351.76 s mz545.27303rt7.97 545.273030 7.970000 3768
#> 3 365.28353 Da 397.38 s mz366.29238rt6.11 366.292380 6.110000 6302
#> 4 365.28353 Da 397.38 s mz366.29238rt6.11 366.292380 6.110000 6304
#> 5 368.29309 Da 463.53 s mz369.2987rt7.73 369.298700 7.730000 6056
#> query_formula chemical_similarity score collisionenergy instrument
#> 1 0.000000 0.810909 15
#> 2 0.000000 0.805937 15
#> 3 0.000000 0.711204 10.0
#> 4 0.000000 0.719118 10.0
#> 5 0.000000 0.816973
#> instrumenttype comment ionmode ccs
#> 1 LC-ESI-ITFT registered in MassBank Positive -1
#> 2 LC-ESI-ITFT registered in MassBank Positive -1
#> 3 LC-ESI-QQ registered in MassBank Positive 195.1324064
#> 4 LC-ESI-QQ registered in MassBank Positive 195.3074064
#> 5 LC-APPI-QQ registered in MassBank Positive -1
#> smiles
#> 1 OP(O)(=O)OCCC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)F
#> 2 OP(O)(=O)OCCC(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)C(F)(F)F
#> 3 CC(C)=CCNC1=C2N(C=NC2=NC=N1)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O
#> 4 CC(C)=CCNC1=C2N=CN([C@@H]3O[C@H](CO)[C@@H](O)[C@H](O)[C@H]3O)C2=NC=N1
#> 5 CC(C)CCCC(C)C1CCC2C3CC[C@@H]4CC(=O)CCC4(C)C3CCC12C
#> inchikey retentiontime precursortype num.peaks
#> 1 MIABSAQIFYEDJP-UHFFFAOYSA-N [M+H]+ 2
#> 2 MIABSAQIFYEDJP-UHFFFAOYSA-N [M+H]+ 2
#> 3 ORUWKZNXHJIZKV-HDNYONAXSA-N [M+H]+ 3
#> 4 XEHLLUQVSRLWMH-HDNYONAXSA-N [M+H]+ 3
#> 5 PESKGJQREUXSRR-JAGYRSRJSA-N [M-H2O+H]+ 3
#> name
#> 1 Perfluorodecyl phosphate; LC-ESI-ITFT; MS2; CE
#> 2 Perfluorodecyl phosphate; LC-ESI-ITFT; MS2; CE
#> 3 N6-Isopentenyladenine-7-glucoside; LC-ESI-QQ; MS2; CE
#> 4 N6-Isopentenyladenine-9-glucoside; LC-ESI-QQ; MS2; CE
#> 5 Coprostanone; LC-APPI-QQ; MS2; CE
#> ontology precursormz formula omu
#> 1 Monoalkyl phosphates 544.980501 C10H6F17O4P omu56
#> 2 Monoalkyl phosphates 544.980501 C10H6F17O4P omu56
#> 3 Glycosylamines 366.177195 C16H23N5O5 omu56
#> 4 Glycosylamines 366.177195 C16H23N5O5 omu56
#> 5 Cholesterols and derivatives 369.351578 C27H46O omu56Ecological Analysis
After your data is processed with our clustering algorithm, we can
start to analyze your data with community metrics. To begin, you have to
create a “community_object”. A community object is a Rcpp Object used
for all ecological analyses. You can generate a “community_object” by
running the create_community_matrix_object(). Once your
object is created, we can start computing the diversity inside of the
samples. We can compute beta (dist_shared()) and alpha
diversity (alpha_summary()). For more information and how
to analyze beta and alpha diversities, continue reading below.
Create the community object/matrix
NNow that the metabolomic features have been clustered into OMUs, it
is possible to use the abundance of each OMU across samples to perform
ecological analyses. First, it is necessary to transform it using the
create_community_matrix_object() function. This will create
a Rcpp object that contains all of your generated ecological data. If
you wish to see what your data looks like, you can call the
get_community_matrix() function.
Packages like vegan opt for using a matrix object as input for
ecological analyses (see more vegan::rarefy()). However, if
we were to use the same methodology, the computation would take far too
long, in particular for the rarefaction algorithm. Rarefaction is the
process of randomly selecting n number of samples without replacement,
with n being the user defined sum threshold. However, in mass
spectrometry, in order to account for machine limits and background
noise, we have to define a sample threshold. After selecting n number of
samples, we only add the samples that are above the size threshold. If
the total is below the sum threshold, we continue until we are equal to
or above the sum threshold. Therefore, adding the sample threshold adds
another layer of complexity to the algorithm. In order to retain
efficiency, we create a custom object that contains all of the necessary
data for the calculation.
community_w_omus <- create_community_matrix_object(data = cluster_results)
community_w_omus
#> omu1 omu2 omu3 omu4 omu5
#> 221012_DGM_Blank4_1_2_435 0.00 0.00 0.00 0.00 0.00
#> omu6 omu7 omu8 omu9 omu10
#> 221012_DGM_Blank4_1_2_435 0.0 0.0 0.00 0.000 0.00
#> omu11 omu12 omu13 omu14 omu15
#> 221012_DGM_Blank4_1_2_435 0.00 0.00 0.00 0.00 0.00
#> [ reached 'max' / getOption("max.print") -- omitted 44 rows and 106 columns ]You have the option of not clustering your data to generate a community object as well. However, by not creating OMUs, it may be more difficult to determine unknown metabolites. Creating OMUs allows users to cluster similar spectra together which means similar features stay together for the community analyses.
community_wo_omus <- create_community_matrix_object(data = matched_data)
community_wo_omus
#> 1000.54504 Da 353.23 s 1001.54432 Da 354.35 s
#> 221012_DGM_Blank1_1_1_390 0.0 0.00
#> 1007.58494 Da 332.99 s 1028.72044 Da 383.88 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.00
#> 1045.57237 Da 354.13 s 1046.70233 Da 400.23 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.00
#> 1050.56754 Da 368.94 s 1061.59820 Da 352.58 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.0
#> 1066.55379 Da 352.85 s 1067.55304 Da 352.68 s
#> 221012_DGM_Blank1_1_1_390 0.0 0.00
#> 1071.29741 Da 576.91 s 1071.30015 Da 562.34 s
#> 221012_DGM_Blank1_1_1_390 0.000 0.0000
#> 1071.30332 Da 476.90 s 1072.29636 Da 562.42 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.0000
#> 1072.30288 Da 475.93 s 1072.30310 Da 484.44 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.00
#> 1072.74610 Da 382.97 s 1073.29826 Da 560.08 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.0000
#> 1073.30391 Da 481.38 s 1076.25679 Da 479.00 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.00
#> 1083.57570 Da 350.99 s 1086.75641 Da 398.91 s
#> 221012_DGM_Blank1_1_1_390 0.0 0.00
#> 1088.53252 Da 351.76 s 1089.59728 Da 354.07 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.00
#> 1090.73035 Da 399.68 s 1090.73102 Da 379.03 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.000
#> 1105.62322 Da 351.91 s 1106.62388 Da 352.21 s
#> 221012_DGM_Blank1_1_1_390 0.0 0.00
#> 1110.57917 Da 351.79 s 1112.66289 Da 331.88 s
#> 221012_DGM_Blank1_1_1_390 0.00 0.0
#> [ reached 'max' / getOption("max.print") -- omitted 44 rows and 644 columns ]Community Matrix
The vegan package uses an object called a “community matrix.” A
community matrix is a matrix that represents samples as rows, and
species as columns. Vegan does not account for machine limits and
background noise, so there is no threshold needed when vegan rarefies
data. In an effort to make a fast and efficient tool, we have opted to
create a community object. It is the same as a community matrix, but it
is created and held in an Rcpp class for speedy access. However, if you
wish to use vegan for other analyses, we have created a
get_community_matrix() function. This function will convert
your community object into a community matrix for ease of use.
get_community_matrix(community_object = community_w_omus)
#> omu1 omu2 omu3 omu4 omu5
#> 221012_DGM_Blank4_1_2_435 0.00 0.00 0.00 0.00 0.00
#> omu6 omu7 omu8 omu9 omu10
#> 221012_DGM_Blank4_1_2_435 0.0 0.0 0.00 0.000 0.00
#> omu11 omu12 omu13 omu14 omu15
#> 221012_DGM_Blank4_1_2_435 0.00 0.00 0.00 0.00 0.00
#> omu16 omu17 omu18 omu19 omu20
#> 221012_DGM_Blank4_1_2_435 0.00 0.000 0.00 0.000 0.00
#> omu21 omu22 omu23 omu24 omu25
#> 221012_DGM_Blank4_1_2_435 0.000 0.000 0.00 0.00 0.000
#> omu26 omu27 omu28 omu29 omu30
#> 221012_DGM_Blank4_1_2_435 0.00 0.00 0.000 0.00 0.000
#> [ reached 'max' / getOption("max.print") -- omitted 44 rows and 91 columns ]Alpha Diversity
Using your created community object, you can compute alpha diversity. Alpha diversity represents diversity (or richness) on a local scale. In our case, it represents the diversity inside of a single sample. You can determine alpha diversity in this package using two different methods: Simpson’s and Shannon’s diversity. Simpson’s diversity represents the diversity on a scale of zero to one, zero meaning no diversity and one meaning maximum diversity. Shannon’s diversity is not bound by zero or one; essentially, the higher the value, the more diversity there is in a single sample.
alpha_summary(community_object = community_w_omus, size = 4000, threshold = 100,
diversity_index = c("simpson", "shannon", "richness"), subsample = TRUE)
#> Computing | 0% ETA: -...Computing ■ | 1% ETA: ...Computing ■■ | 3% ETA: ...Computing ■■■ | 5% ETA: ...Computing ■■■■ | 7% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 11% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 15% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 21% ETA: ...Computing ■■■■■■■■■■■■ | 23% ETA: ...Computing ■■■■■■■■■■■■■ | 25% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 31% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 37% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 41% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 43% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 47% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 51% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 57% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 63% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 69% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 75% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 81% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 83% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 87% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 89% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 93% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 95% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
#> samples simpson shannon
#> 221012_DGM_Blank4_1_2_435 221012_DGM_Blank4_1_2_435 0.6095089 0.9401740
#> 221012_DGM_Blank4_1_1_434 221012_DGM_Blank4_1_1_434 0.6201988 0.9679359
#> 221012_DGM_MB1599_13_3_433 221012_DGM_MB1599_13_3_433 0.2965709 0.3522099
#> richness
#> 221012_DGM_Blank4_1_2_435 6.00
#> 221012_DGM_Blank4_1_1_434 6.00
#> 221012_DGM_MB1599_13_3_433 4.69
#> [ reached 'max' / getOption("max.print") -- omitted 42 rows ]Beta Diversity
Beta diversity values can be calculated using the Bray-Curtis,
Theta-YC, Jaccard, Hamming, Moristia-Horn, or Sorenson distance
calculators. Users are strongly encouraged to use rarefaction to control
for uneven sampling effort when calculating any diversity metric. By
default, the dist_shared() function uses subsample = TRUE,
which automatically rarefies the samples.
Beta diversity represents the dissimilarity between different samples. With this calculation the user can generate distances between the community that can be used for visualizations. And, with all of the annotations and clusters that were computed earlier, you can see how dissimilar/similar the samples are.
Below are examples of using rarefaction to calculate Bray-Curtis distances using OMU or individual metabolites.
bray_w_omus <- dist_shared(community_object = community_w_omus, size = 4000,
threshold = 100, diversity_index = "bray", subsample = TRUE)
#> Computing | 0% ETA: -...Computing ■ | 1% ETA: ...Computing ■■ | 3% ETA: ...Computing ■■■ | 5% ETA: ...Computing ■■■■ | 7% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 11% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 15% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 21% ETA: ...Computing ■■■■■■■■■■■■ | 23% ETA: ...Computing ■■■■■■■■■■■■■ | 25% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 31% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 37% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 41% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 43% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 47% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 51% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 57% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 63% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 69% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 75% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 81% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 83% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 87% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 89% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 93% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 95% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
bray_w_omus
#> 221012_DGM_Blank4_1_2_435 221012_DGM_Blank4_1_1_434
#> 221012_DGM_Blank4_1_1_434 0.02407000
#> 221012_DGM_MB1599_13_3_433
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1599_13_1_431
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1598_12_3_430
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1598_12_1_428
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1597_11_2_426
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1595_10_3_424
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1595_10_2_423
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1597_11_3_427
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_MB1595_10_1_422 221012_DGM_Blank2_1_1_404
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_Blank3_1_1_419 221012_DGM_MB1590_5_3_403
#> 221012_DGM_Blank4_1_1_434
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_Blank4_1_1_434
#> [ reached 'max' / getOption("max.print") -- omitted 43 rows and 29 columns ]
bray_no_omus <- dist_shared(community_object = community_wo_omus, size = 4000,
threshold = 100, diversity_index = "bray", subsample = TRUE)
#> Computing | 0% ETA: -...Computing ■ | 1% ETA: ...Computing ■■ | 3% ETA: ...Computing ■■■ | 5% ETA: ...Computing ■■■■ | 7% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 11% ETA: 7s ...Computing ■■■■■■■ | 14% ETA: 6s ...Computing ■■■■■■■■ | 15% ETA: 5s ...Computing ■■■■■■■■■ | 18% ETA: 4s ...Computing ■■■■■■■■■■ | 20% ETA: 3s ...Computing ■■■■■■■■■■■ | 21% ETA: 3s ...Computing ■■■■■■■■■■■■ | 23% ETA: 3s ...Computing ■■■■■■■■■■■■■ | 25% ETA: 2s ...Computing ■■■■■■■■■■■■■■ | 28% ETA: 2s ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: 2s ...Computing ■■■■■■■■■■■■■■■■ | 31% ETA: 2s ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■ | 37% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 41% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 43% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 47% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: 1s ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 51% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 57% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 63% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 69% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 75% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 81% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 83% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 87% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 89% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 93% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 95% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
bray_no_omus
#> 221012_DGM_Blank1_1_1_390 221012_DGM_Blank1_1_2_391
#> 221012_DGM_Blank1_1_2_391 0.06219456
#> 221012_DGM_Blank1_1_3_392 221012_DGM_MB1588_3_1_395
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_MB1588_3_2_396 221012_DGM_MB1588_3_3_397
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_MB1589_4_1_398 221012_DGM_MB1589_4_2_399
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_MB1589_4_3_400 221012_DGM_MB1590_5_1_401
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_MB1590_5_2_402 221012_DGM_MB1590_5_3_403
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_Blank2_1_1_404 221012_DGM_Blank2_1_2_405
#> 221012_DGM_Blank1_1_2_391
#> 221012_DGM_Blank2_1_3_406
#> 221012_DGM_Blank1_1_2_391
#> [ reached 'max' / getOption("max.print") -- omitted 43 rows and 29 columns ]Visualizations
There are a few different ways to visualize the data generated from this package. Below we have examples of a PCOA plot, Hierarchical Clustering graph, Network graph, and Box plot.
PCOA
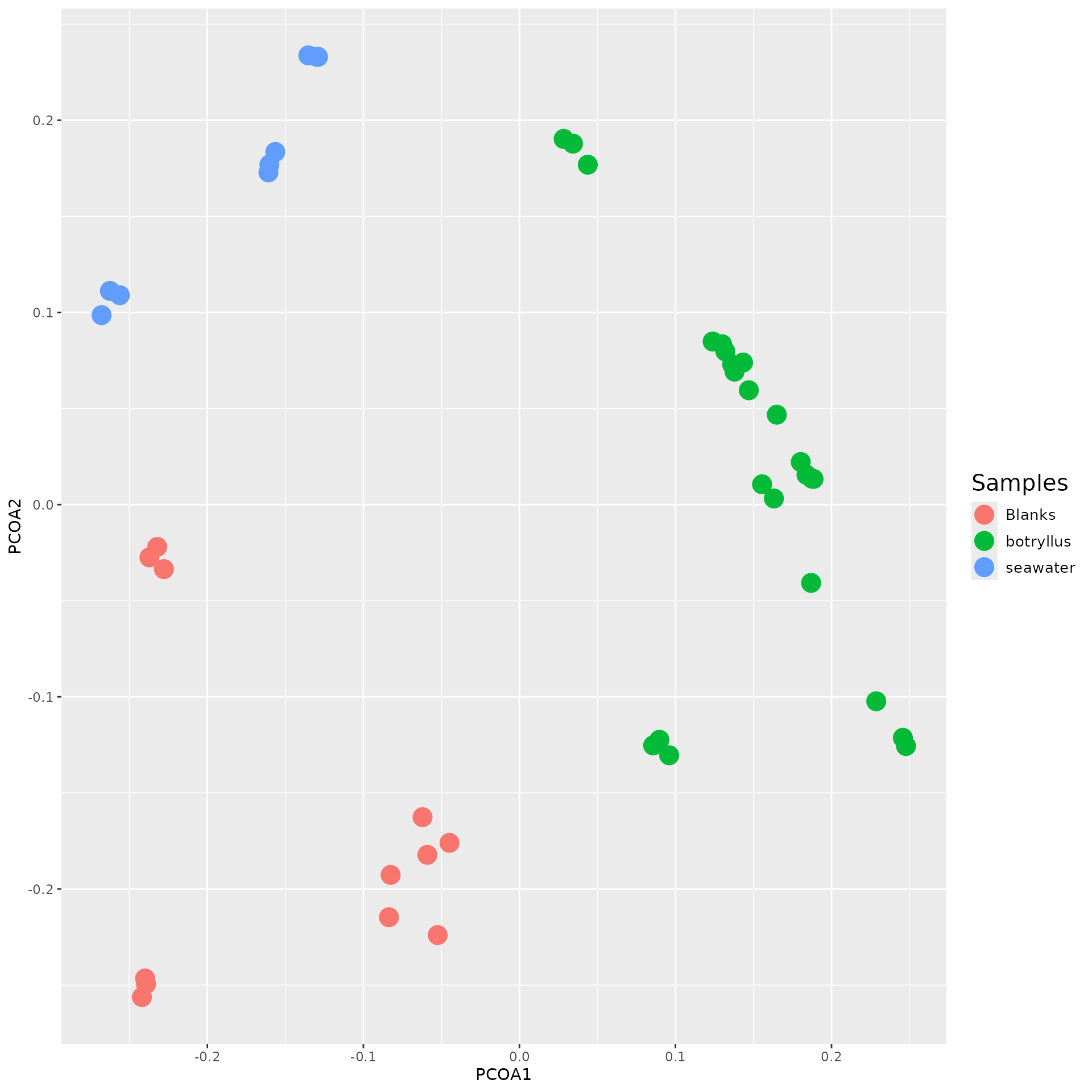
Principal Coordinate Analysis (PCOA) is a statistical technique used
to show similarities between data. PCOA allows us, in particular, to use
the distances generated from our ecological analysis. And, unlike
Principle Component Analysis (PCA), it is not limited to only euclidean
distances. So, we can use the distances generated from
dist_shared() as input for this calculation. To start, we
need to convert the dist_shared() result into cartisan
coordinates. To do this, we can use the stats::cmdscale()
function. Then, we can extract the points from the
stats::cmdscale() function and rename them to be more
readable. Finally, we plot the values. PCOA is a great way to look at
your beta diversity results visually and shows us how similar samples
are to each other.
dist_obj <- bray_w_omus
pcoa <- cmdscale(dist_obj, k = 2, eig = T, add = T)
pcoa_points <- as.data.frame(pcoa$points)
variance <- round(pcoa$eig*100/sum(pcoa$eig), 1)
names(pcoa_points) <- paste0("PCOA", seq(1:2))
pcoa_points$Samples <- rownames(pcoa_points)
meta_data <- get_meta_data(filtered_data)
for(i in 1:nrow(pcoa_points)) {
idx <- which(pcoa_points$Samples[[i]] == meta_data$Injection)
pcoa_points$Samples[[i]] <- meta_data$Biological_Group[[idx]]
}
pcoa_points |>
ggplot(aes(x=PCOA1, y = PCOA2, color = Samples)) +
geom_point(size = 5.5) +
theme(
legend.text = element_text(size = 10),
legend.title = element_text(size = 15)
)
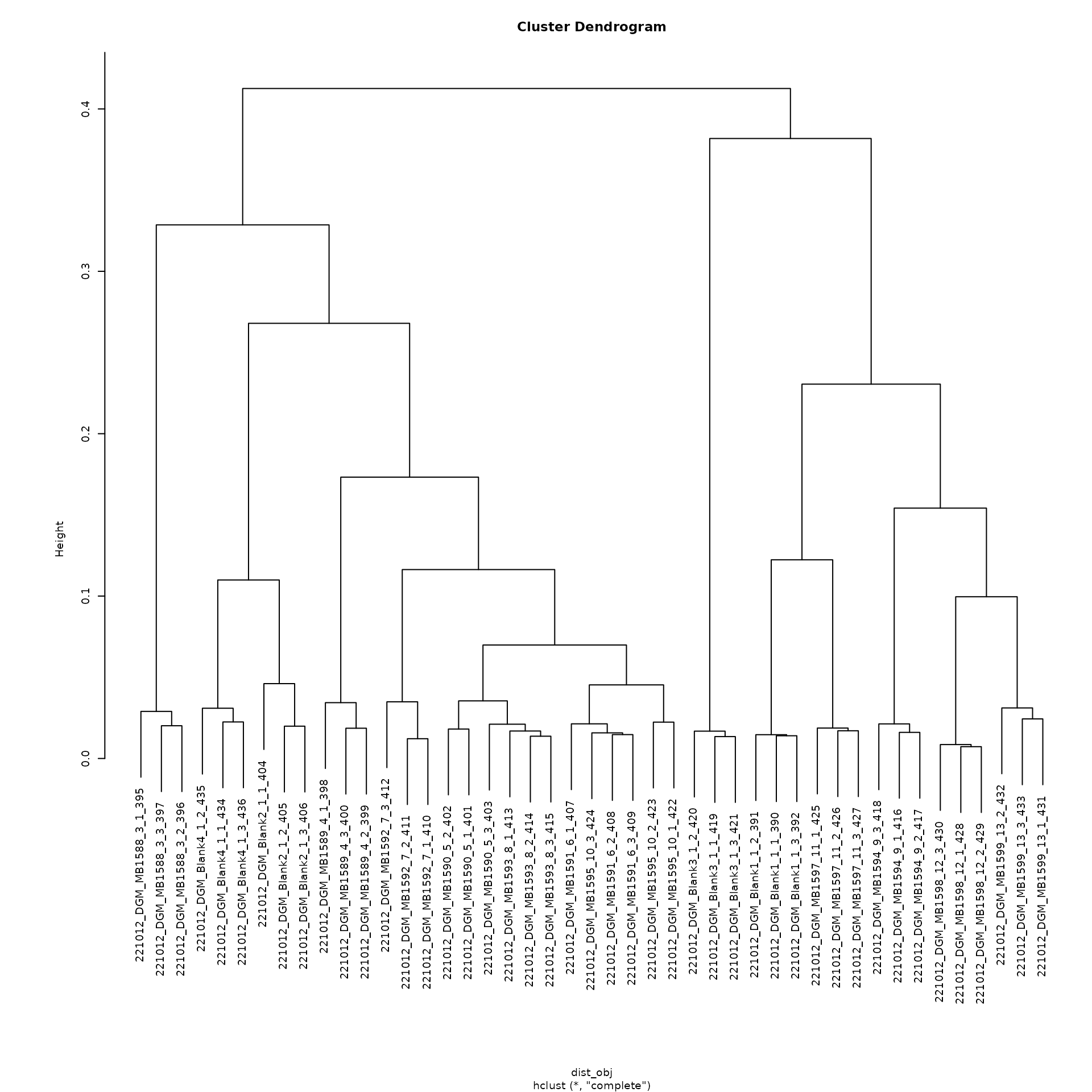
Hierarchical Clustering
Another visualization approach is to perform hierarchical clustering
using the stats::hclust() function. Hierarchical clustering
generates a tree of samples based on their beta diversity values to show
the similarities of the samples. The results are similar to that of PCoA
but it uses a tree like structure to showcase relationships. It tends to
be easier to look at relationships or clusters using this type of
graph.
Network Plot
Sometimes, it is useful to see a visual map of your annotations. We
can accomplish this using a network plot. By creating a network of data,
we can see which annotations matched certain features. Using
networkD3::simpleNetwork(), we can generate a simple
network plot.
distance_df_annotations <- annotations[, c("query_ms2_id", "name", "score")]
simpleNetwork(distance_df_annotations, height="100px", width="100px", zoom = TRUE)Using Group Averages
Another feature included inside of mums2 is the ability to run your
analysis using group averages. Some researchers conduct mass
spectrometry experiments by running samples in technical/injection
triplicate to account for instrument variability. Since we know all
three injections are from the same vial, we can average all of these
into one group. We can generate group averages by using the metadata
file that was supplied when you imported your data based on
“Sample_Code”. We can accomplish this by using the
convert_to_group_averages() function.
Below, you can see a copy of the alpha and beta diversity functions we ran above. But this time, we are using group averages.
matched_avg <- convert_to_group_averages(matched_data = matched_data, mpactr_object = filtered_data)
dist_avg <- dist_ms2(
data = matched_avg, cutoff = 0.3, precursor_thresh = 2,
score_params = modified_cosine_params(0.5), min_peaks = 0)
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
cluster_results_avg <- cluster_data(
distance_df = dist, ms2_match_data = matched_avg, cutoff = 0.3,
cluster_method = "opticlust")
annotations_avg <- annotate_ms2(mass_data = matched_avg, reference = reference_db, scoring_params = modified_cosine_params(0.5),
ppm = 1000, min_score = 0.6, chemical_min_score = 0, cluster_data = cluster_results_avg)
#> Computing | 0% ETA: -...Computing ■ | 2% ETA: ...Computing ■■ | 4% ETA: ...Computing ■■■ | 6% ETA: ...Computing ■■■■ | 8% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 12% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 16% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 22% ETA: ...Computing ■■■■■■■■■■■■ | 24% ETA: ...Computing ■■■■■■■■■■■■■ | 26% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 32% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 38% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 42% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 44% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 48% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 52% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 58% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 64% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 70% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 76% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 78% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 82% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 84% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 88% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 90% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 94% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 96% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
community_object_avg <- create_community_matrix_object(data = cluster_results_avg)
head(get_community_matrix(community_object = community_object_avg), 3)
#> omu1 omu2 omu3 omu4 omu5 omu6 omu7 omu8 omu9 omu10 omu11 omu12
#> blank3 0.00 0.0 0 0.0 0 0 0 0 0 0 0 0
#> MB1589 23337.03 24115.4 0 14022.7 0 0 0 0 0 0 0 0
#> MB1588 0.00 0.0 0 0.0 0 0 0 0 0 0 0 0
#> omu13 omu14 omu15 omu16 omu17 omu18 omu19 omu20 omu21
#> blank3 0 0 0 0.00 0.0 0.0 0 0 0.000
#> MB1589 0 0 0 42087.33 10749.4 127599.7 0 0 8942.717
#> MB1588 0 0 0 0.00 0.0 0.0 0 0 0.000
#> omu22 omu23 omu24 omu25 omu26 omu27 omu28 omu29 omu30
#> blank3 0.000 0 0 0.000 0.00 0 0.00 0.00 0
#> MB1589 7274.027 0 0 5316.441 73722.57 0 67484.12 35960.23 0
#> MB1588 0.000 0 0 0.000 0.00 0 0.00 0.00 0
#> omu31 omu32 omu33 omu34 omu35 omu36 omu37 omu38 omu39
#> blank3 0.00 0.000 0.00 0 0.00 0 0 0.000 0
#> MB1589 61818.83 8703.846 29907.96 0 28524.01 0 0 8212.385 0
#> MB1588 0.00 0.000 0.00 0 0.00 0 0 0.000 0
#> omu40 omu41 omu42 omu43 omu44 omu45 omu46 omu47 omu48 omu49 omu50
#> blank3 0 0 0 0 0 0 0.000 0 0 0.00 0
#> MB1589 0 0 0 0 0 0 9891.063 0 0 31016.72 0
#> MB1588 0 0 0 0 0 0 0.000 0 0 0.00 0
#> omu51 omu52 omu53 omu54 omu55 omu56 omu57 omu58 omu59
#> blank3 0.0 0 0 0.00 0 536344.8 0.00 0.00 0
#> MB1589 18200.5 0 0 60820.68 0 11950209.3 10110.24 98530.36 0
#> MB1588 0.0 0 0 212704.06 0 2761290.9 0.00 479136.87 0
#> omu60 omu61 omu62 omu63 omu64 omu65 omu66 omu67 omu68 omu69
#> blank3 0 0 71059.94 0.00 0.00 0.0 0 0 0 0
#> MB1589 0 0 578187.41 11067.09 20210.32 11347.3 0 0 0 0
#> MB1588 0 0 0.00 0.00 0.00 0.0 0 0 0 0
#> omu70 omu71 omu72 omu73 omu74 omu75 omu76 omu77
#> blank3 0.000 0 0.000 65837.39 4293.939 0.00 0 0.00
#> MB1589 210327.208 0 7873.674 5096777.02 217270.654 49602.83 0 67868.33
#> MB1588 6803.707 0 0.000 1098725.26 15809.002 27996.26 0 0.00
#> omu78 omu79 omu80 omu81 omu82 omu83 omu84 omu85
#> blank3 0.00 0 0 0 101080.8 4267.063 0.00 0.00
#> MB1589 83334.29 0 0 0 2751336.9 28711.179 96614.68 61664.97
#> MB1588 0.00 0 0 0 0.0 0.000 0.00 138083.00
#> omu86 omu87 omu88 omu89 omu90 omu91 omu92 omu93 omu94
#> blank3 98687.36 0 4669.115 0.00 0 0.00 0.00 0 0
#> MB1589 322682.14 0 23251.863 19642.83 0 57334.46 38534.01 0 0
#> MB1588 260084.95 0 0.000 0.00 0 0.00 0.00 0 0
#> omu95 omu96 omu97 omu98 omu99 omu100 omu101 omu102
#> blank3 0.00 7709.688 0.0 0.0 37381.96 0 0 0
#> MB1589 62575.24 278049.688 804098.7 37879.9 166117.64 0 0 0
#> MB1588 0.00 0.000 0.0 0.0 26708.77 0 0 0
#> omu103 omu104 omu105 omu106 omu107 omu108 omu109 omu110 omu111
#> blank3 0 0 0 0.00 0 4068.33 0 0.00 0
#> MB1589 0 0 0 12633.89 0 118577.04 0 38765.94 0
#> MB1588 0 0 0 0.00 0 0.00 0 46022.30 0
#> omu112 omu113 omu114 omu115 omu116 omu117 omu118 omu119 omu120
#> blank3 0 0 0.00 0.00 0 0 0 0 0
#> MB1589 0 0 73379.17 15677.16 0 0 0 0 0
#> MB1588 0 0 90119.16 0.00 0 0 0 0 0
#> omu121
#> blank3 0
#> MB1589 0
#> MB1588 0You can also see how the samples in the matched object have been adjusted based on the information supplied in the metadata file.
# Normal
head(matched_data$samples)
#> [1] "221012_DGM_Blank1_1_1_390" "221012_DGM_Blank1_1_2_391"
#> [3] "221012_DGM_Blank1_1_3_392" "221012_DGM_MB1588_3_1_395"
#> [5] "221012_DGM_MB1588_3_2_396" "221012_DGM_MB1588_3_3_397"
# Group Average
head(matched_avg$samples)
#> [1] "blank" "MB1588" "MB1589" "MB1590" "blank1" "MB1591"
# The items in the Injection have been converted into the corresponding sample code.
get_meta_data(filtered_data)[, c("Injection", "Sample_Code")]
#> Injection Sample_Code
#> <char> <char>
#> 1: 221012_DGM_Blank1_1_1_390 blank
#> 2: 221012_DGM_Blank1_1_2_391 blank
#> 3: 221012_DGM_Blank1_1_3_392 blank
#> 4: 221012_DGM_MB1588_3_1_395 MB1588
#> 5: 221012_DGM_MB1588_3_2_396 MB1588
#> 6: 221012_DGM_MB1588_3_3_397 MB1588
#> 7: 221012_DGM_MB1589_4_1_398 MB1589
#> 8: 221012_DGM_MB1589_4_2_399 MB1589
#> 9: 221012_DGM_MB1589_4_3_400 MB1589
#> 10: 221012_DGM_MB1590_5_1_401 MB1590
#> 11: 221012_DGM_MB1590_5_2_402 MB1590
#> 12: 221012_DGM_MB1590_5_3_403 MB1590
#> 13: 221012_DGM_Blank2_1_1_404 blank1
#> 14: 221012_DGM_Blank2_1_2_405 blank1
#> 15: 221012_DGM_Blank2_1_3_406 blank1
#> 16: 221012_DGM_MB1591_6_1_407 MB1591
#> 17: 221012_DGM_MB1591_6_2_408 MB1591
#> 18: 221012_DGM_MB1591_6_3_409 MB1591
#> 19: 221012_DGM_MB1592_7_1_410 MB1592
#> 20: 221012_DGM_MB1592_7_2_411 MB1592
#> 21: 221012_DGM_MB1592_7_3_412 MB1592
#> 22: 221012_DGM_MB1593_8_1_413 MB1593
#> 23: 221012_DGM_MB1593_8_2_414 MB1593
#> 24: 221012_DGM_MB1593_8_3_415 MB1593
#> 25: 221012_DGM_MB1594_9_1_416 MB1594
#> 26: 221012_DGM_MB1594_9_2_417 MB1594
#> 27: 221012_DGM_MB1594_9_3_418 MB1594
#> 28: 221012_DGM_Blank3_1_1_419 blank2
#> 29: 221012_DGM_Blank3_1_2_420 blank2
#> 30: 221012_DGM_Blank3_1_3_421 blank2
#> 31: 221012_DGM_MB1595_10_1_422 MB1595
#> 32: 221012_DGM_MB1595_10_2_423 MB1595
#> 33: 221012_DGM_MB1595_10_3_424 MB1595
#> 34: 221012_DGM_MB1597_11_1_425 MB1597
#> 35: 221012_DGM_MB1597_11_2_426 MB1597
#> 36: 221012_DGM_MB1597_11_3_427 MB1597
#> 37: 221012_DGM_MB1598_12_1_428 MB1598
#> 38: 221012_DGM_MB1598_12_2_429 MB1598
#> 39: 221012_DGM_MB1598_12_3_430 MB1598
#> 40: 221012_DGM_MB1599_13_1_431 MB1599
#> 41: 221012_DGM_MB1599_13_2_432 MB1599
#> 42: 221012_DGM_MB1599_13_3_433 MB1599
#> 43: 221012_DGM_Blank4_1_1_434 blank3
#> 44: 221012_DGM_Blank4_1_2_435 blank3
#> 45: 221012_DGM_Blank4_1_3_436 blank3
#> Injection Sample_Code
#> <char> <char>Combined data frames
mums2 also allows you to view your all of your generated data
together using the generate_a_combined_table() function.
This function will take your matched object (generated from
ms2_ms1_compare()), your annotations object (generated from
annotate_ms2()) and your cluster data (generated from
cluster_data()) to generate a combined data.frame with all
of the generated data.
# For normal data
head(generate_a_combined_table(matched_data = matched_data, annotations = annotations, cluster_data = cluster_results), 3)
#> ms1_id ms2_id mz RTINMINUTES omus
#> 1 1000.05311 Da 399.15 s 1001.06039 6.65
#> 2 1000.20067 Da 536.14 s 1001.20795 8.94
#> 3 1000.54504 Da 353.23 s mz1023.53293rt5.89 1023.53397 5.89 omu56
#> annotations 221012_DGM_Blank1_1_1_390 221012_DGM_Blank1_1_2_391
#> 1 <NA> 0 0
#> 2 <NA> 0 0
#> 3 <NA> 0 0
#> 221012_DGM_Blank1_1_3_392 221012_DGM_Blank2_1_1_404 221012_DGM_Blank2_1_2_405
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_Blank2_1_3_406 221012_DGM_Blank3_1_1_419 221012_DGM_Blank3_1_2_420
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_Blank3_1_3_421 221012_DGM_Blank4_1_1_434 221012_DGM_Blank4_1_2_435
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_Blank4_1_3_436 221012_DGM_MB1588_3_1_395 221012_DGM_MB1588_3_2_396
#> 1 0 0 0
#> 2 0 13693.07422 16856.57227
#> 3 0 0 0
#> 221012_DGM_MB1588_3_3_397 221012_DGM_MB1589_4_1_398 221012_DGM_MB1589_4_2_399
#> 1 0 0 0
#> 2 16332.37109 0 0
#> 3 0 0 0
#> 221012_DGM_MB1589_4_3_400 221012_DGM_MB1590_5_1_401 221012_DGM_MB1590_5_2_402
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_MB1590_5_3_403 221012_DGM_MB1591_6_1_407 221012_DGM_MB1591_6_2_408
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_MB1591_6_3_409 221012_DGM_MB1592_7_1_410 221012_DGM_MB1592_7_2_411
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_MB1592_7_3_412 221012_DGM_MB1593_8_1_413 221012_DGM_MB1593_8_2_414
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_MB1593_8_3_415 221012_DGM_MB1594_9_1_416 221012_DGM_MB1594_9_2_417
#> 1 0 0 0
#> 2 0 0 0
#> 3 0 0 0
#> 221012_DGM_MB1594_9_3_418 221012_DGM_MB1595_10_1_422
#> 1 0 0
#> 2 0 0
#> 3 0 0
#> 221012_DGM_MB1595_10_2_423 221012_DGM_MB1595_10_3_424
#> 1 0 0
#> 2 0 0
#> 3 0 0
#> 221012_DGM_MB1597_11_1_425 221012_DGM_MB1597_11_2_426
#> 1 15105.3584 13140.04102
#> 2 0 0
#> 3 168557.4844 176505.7656
#> 221012_DGM_MB1597_11_3_427 221012_DGM_MB1598_12_1_428
#> 1 17551.48633 0
#> 2 0 0
#> 3 160923.4531 0
#> 221012_DGM_MB1598_12_2_429 221012_DGM_MB1598_12_3_430
#> 1 0 0
#> 2 0 0
#> 3 0 0
#> 221012_DGM_MB1599_13_1_431 221012_DGM_MB1599_13_2_432
#> 1 13573.70703 13245.09473
#> 2 0 0
#> 3 153978.0625 158672.2344
#> 221012_DGM_MB1599_13_3_433
#> 1 13221.94824
#> 2 0
#> 3 165991.4375
# For group averaged data
head(generate_a_combined_table(matched_data = matched_avg, annotations = annotations_avg, cluster_data = cluster_results_avg), 3)
#> ms1_id ms2_id mz RTINMINUTES omus
#> 1 1000.05311 Da 399.15 s 1001.06039 6.65
#> 2 1000.20067 Da 536.14 s 1001.20795 8.94
#> 3 1000.54504 Da 353.23 s mz1023.53293rt5.89 1023.53397 5.89 omu56
#> annotations blank MB1588 MB1589 MB1590 blank1 MB1591 MB1592 MB1593
#> 1 <NA> 0 0 0 0 0 0 0 0
#> 2 <NA> 0 15627.3391933333 0 0 0 0 0 0
#> 3 <NA> 0 0 0 0 0 0 0 0
#> MB1594 blank2 MB1595 MB1597 MB1598 MB1599 blank3
#> 1 0 0 0 15265.6285833333 0 13346.9166666667 0
#> 2 0 0 0 0 0 0 0
#> 3 0 0 0 168662.234366667 0 159547.2448 0Heat map
Another way to visualize diversity data is to use a heat map. We can easily see how correlated data is between samples with a heatmap.
dist_shared(community_object_avg, 4000, 100, "jaccard") |>
as.matrix() |>
reshape2::melt(varnames = c("A", "B"), value.name = "distances") |>
ggplot(aes(x = A, y = B, fill = distances)) +
geom_tile() +
scale_fill_gradient(low="#FF0000", high = "#FFFFFF")
#> Computing | 0% ETA: -...Computing ■ | 1% ETA: ...Computing ■■ | 3% ETA: ...Computing ■■■ | 5% ETA: ...Computing ■■■■ | 7% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 11% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 15% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 21% ETA: ...Computing ■■■■■■■■■■■■ | 23% ETA: ...Computing ■■■■■■■■■■■■■ | 25% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 31% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 37% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 41% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 43% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 47% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 51% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 57% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 63% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 69% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 75% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 81% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 83% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 87% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 89% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 93% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 95% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...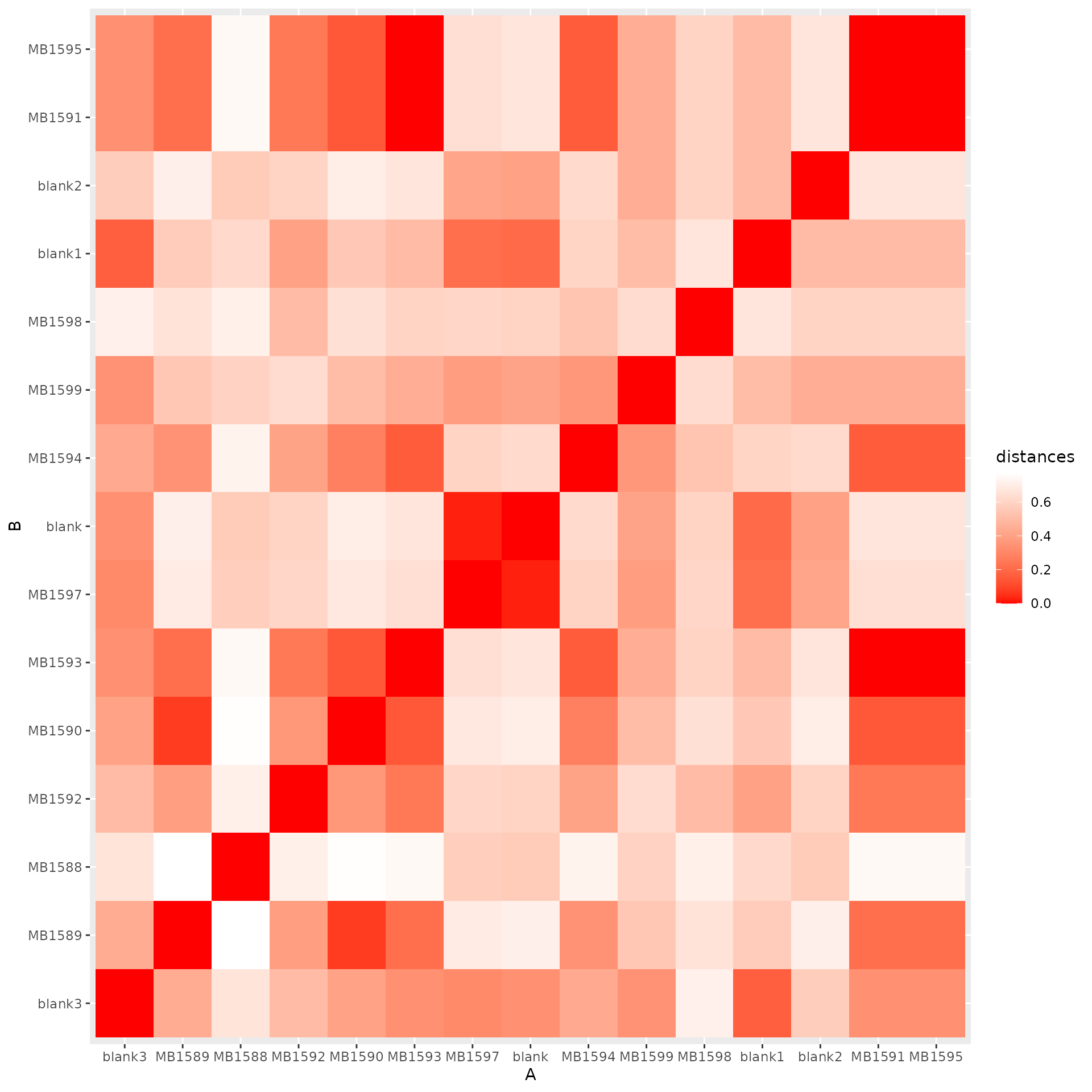
Box Plot
A box and whisker plot can also be used to depict the variation of the data. We can take advantage of this to look at the distributions inside of our generate beta and alpha diversity data. Below is a box plot using alpha diversity.
alpha <- alpha_summary(community_object_avg, 4000, 100, "simpson")
#> Computing | 0% ETA: -...Computing ■ | 1% ETA: ...Computing ■■ | 3% ETA: ...Computing ■■■ | 5% ETA: ...Computing ■■■■ | 7% ETA: ...Computing ■■■■■ | 10% ETA: ...Computing ■■■■■■ | 11% ETA: ...Computing ■■■■■■■ | 14% ETA: ...Computing ■■■■■■■■ | 15% ETA: ...Computing ■■■■■■■■■ | 18% ETA: ...Computing ■■■■■■■■■■ | 20% ETA: ...Computing ■■■■■■■■■■■ | 21% ETA: ...Computing ■■■■■■■■■■■■ | 23% ETA: ...Computing ■■■■■■■■■■■■■ | 25% ETA: ...Computing ■■■■■■■■■■■■■■ | 28% ETA: ...Computing ■■■■■■■■■■■■■■■ | 30% ETA: ...Computing ■■■■■■■■■■■■■■■■ | 31% ETA: ...Computing ■■■■■■■■■■■■■■■■■ | 34% ETA: ...Computing ■■■■■■■■■■■■■■■■■■ | 36% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■ | 37% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■ | 40% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■ | 41% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■ | 43% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■ | 46% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■ | 47% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■ | 50% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■ | 51% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 54% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 56% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 57% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 60% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 62% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 63% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 66% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 68% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 69% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 72% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 74% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 75% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 77% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 80% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 81% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 83% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 86% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 87% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 89% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 92% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 93% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 95% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 98% ETA: ...Computing ■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■■ | 100% ETA: ...
# Convert Sample_Codes into Biological Groups
meta_data <- get_meta_data(filtered_data)
alpha$group <- sapply(alpha$samples, function(x) {
meta_data$Biological_Group[[which(x == meta_data$Sample_Code)[[1]]]]
}, USE.NAMES = FALSE)
# Plot
colnames(alpha) <- c("sample_code", "diversity", "group")
alpha |>
ggplot(aes(x = sample_code, y = diversity, group = group)) +
geom_point() +
geom_boxplot(alpha = 0.3) +
facet_wrap(~group, scales = "free_x")